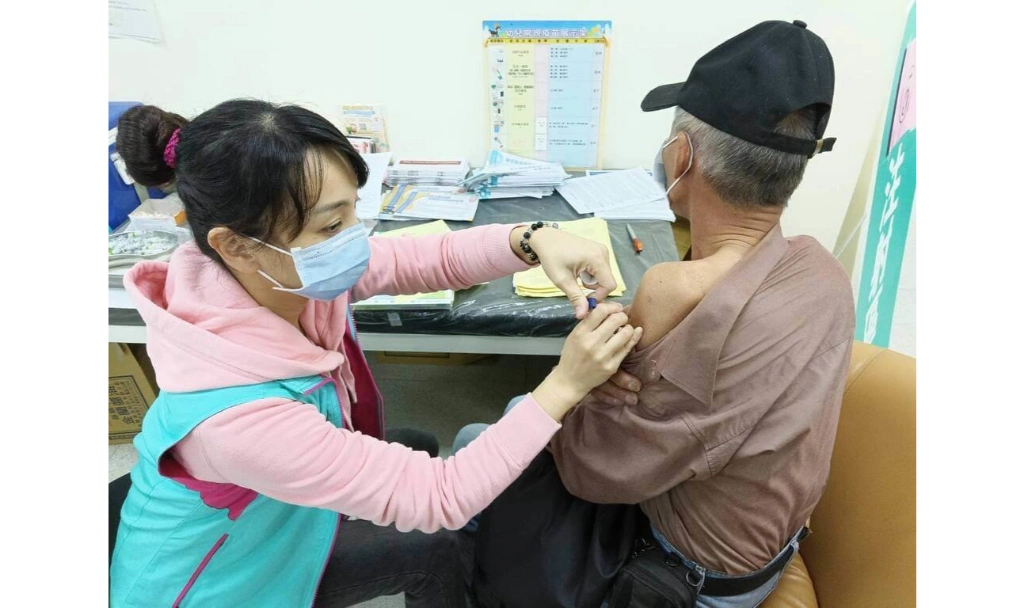
梁賡義指出,在疫情發生初期,產學研界即啟動投入疫苗研發,如國衛院利用4種技術平台同步開發,最快在今(2020)年秋季即可進入人體臨床試驗。
國內武漢肺炎疫情獲得控制,然而國際疫情尚未緩解,武漢肺炎病毒預防及治療疫苗與藥物將是後續防疫工作的重要利器中央流行疫情指揮中心研發組長梁賡義今(3)日表示,考量武漢肺炎疫情恐持續到年底,全球一百多個研究單位持續投入疫苗研發,其中10個疫苗進入臨床試驗;國產疫苗部分,國衛院與中研院亦持續投入疫苗開發,最快今年秋季可進入人體臨床試驗。
梁賡義指出,面對全球性的防疫需求,與其盼望國外能夠供應足夠的疫苗給台灣,我國必須要厚植自製疫苗的能力,以滿足國內的防疫需求,並且兼顧國際防疫合作,因此在疫情發生初期,產學研界即啟動投入疫苗研發,如國衛院利用4種技術平台同步開發,最快在今(2020)年秋季即可進入人體臨床試驗;中研院開發的奈米疫苗,目前也正進行疫苗劑型與劑量的優化。前述兩個研究單位的成果均已與國內廠商洽談並啟動合作。此外,國內廠商所開發的疫苗也預計於今年底前可進入臨床人體試驗。政府也持續提供相關輔導,已大幅縮短疫苗開發時程。
新藥開發方面,梁賡義表示,國內學研界也積極研發治療新型冠狀病毒的候選藥物,例如國衛院團隊已找到具抑制新冠病毒活性的化合物,從初步實驗結果顯示極具有開發的潛力及價值。中研院團隊篩選出新冠病毒主要蛋白酶抑制劑,此強效的蛋白酶抑制劑,可在體外抑制新冠病毒複製。長庚團隊以及國衛院、預醫所團隊也分別找到單株抗體藥物,其抑制新型冠狀病毒能力高達90%以上。
食藥署因應國內緊急公共衛生情事需求,協助疾管署依照藥事法取得疫情初期所需之檢驗試劑專案進口。同時預估疫情發展,超前部署國內檢驗試劑、藥品及疫苗需求,提供廠商依循類似於美國緊急使用授權(EUA)機制,提出檢驗試劑、藥品及疫苗之專案製造及輸入申請,截至目前為止,已核准4件檢驗試劑專案製造及19件檢驗試劑專案輸入。
為積極扶植國內產業研發疫情所需檢驗試劑、藥品及疫苗,成立專業輔導團隊,盤點國內研發量能,提供諮詢輔導專線及專人輔導,提供至少22家廠商檢驗試劑專案製造輔導及10家藥品/疫苗查驗登記輔導。此外,預防疫情再襲,食藥署召開專家會議並依決議核准1件藥品之查驗登記申請。
指揮中心表示,繼口罩國家隊後,科技防疫國家隊亦儼然成形,結合產官學研的儲備量能,因應疫情再次發生時,台灣有足夠的自我保護能力,也能持續對全球防疫有所貢獻。
(記者吳栢妤/攝影)