
研究顯示, 高端疫苗的耐受性良好,大多數的受試者注射後反應報告為輕度,中和抗體幾何平均濃度 (GMT) 與人體恢復血清的GMT水平相當。
國產高端疫苗增開預約至今(25)日下午6點截止,一共逾15.2萬人完成預約,預計27日施打,目前預約高端累計已超過75萬人。日前知名醫學期刊《刺胳針》The Lancet respiratory medicine刊登,以高端疫苗臨床試驗主持人、台大感染科醫師謝思民所主筆的「高端疫苗安全性與免疫性臨床實驗報告」。此論文指出,高端疫苗能引發強大的免疫反應,引起的不良事件大多較為輕微且相似。
論文研究,高端武漢肺炎疫苗(MVC COV1901)的安全性與免疫性,該疫苗由基因重組S-2P棘蛋白技術組成,此技術為美國家過敏症和傳染病研究所 (NIAID) 疫苗研究中心的Barney S. Graham博士使用重組蛋白平台與佐劑CpG 1018結合開發。
研究顯示, 高端疫苗的耐受性良好,大多數的受試者注射後反應報告為輕度,中和抗體幾何平均濃度 (GMT) 與人體恢復血清的GMT水平相當。
論文指出,高端在2020年9月28日至11月13日期間,針對77名參與者進行審查,將其中45名的20~49歲健康成年人在間隔28天分別注射, 5毫克、15毫克、25毫克兩劑高端疫苗。每個劑量組有15名參與者; 在中期分析時,在第二次給藥後對所有患者進行28天的追蹤,記錄不良事件、數據作為安全性評估,同時在不同時間點收集血樣來觀測細胞免疫反應。
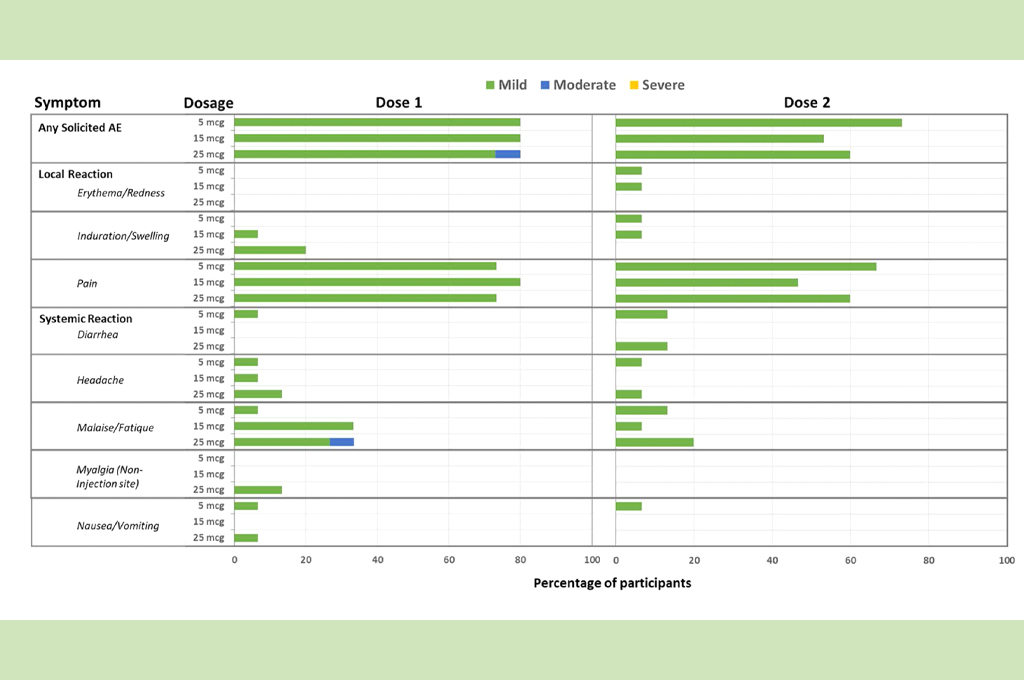
研究發現,高端疫苗所引起的不良事件(AE)大多「輕微」且「相似」,沒有任何受試者有發燒的情況。
安全性方面,研究顯示,在該數據截止點的2020年12月23日,未發生嚴重不良事件(SAE)或特別關注不良事件(AESI)。在所有治療組中,出現局部不良事件(AE)為80.0%的疼痛與酸痛;全身性不良事件則為28.9%的不適與疲勞。除了在25毫克的劑量組中有一1例全身不適且疲勞,所有局部、全身的不良事件皆為輕度反應。
「沒有參與者發燒。」研究指出,高端疫苗在第一次和第二次給藥後引起的不良事件相似。 安全實驗室值、心電圖顯示和受試者提供的不良事件評估報告皆無顯示具體問題。 31.1%參與者的抗核抗體增加,且均無症狀。
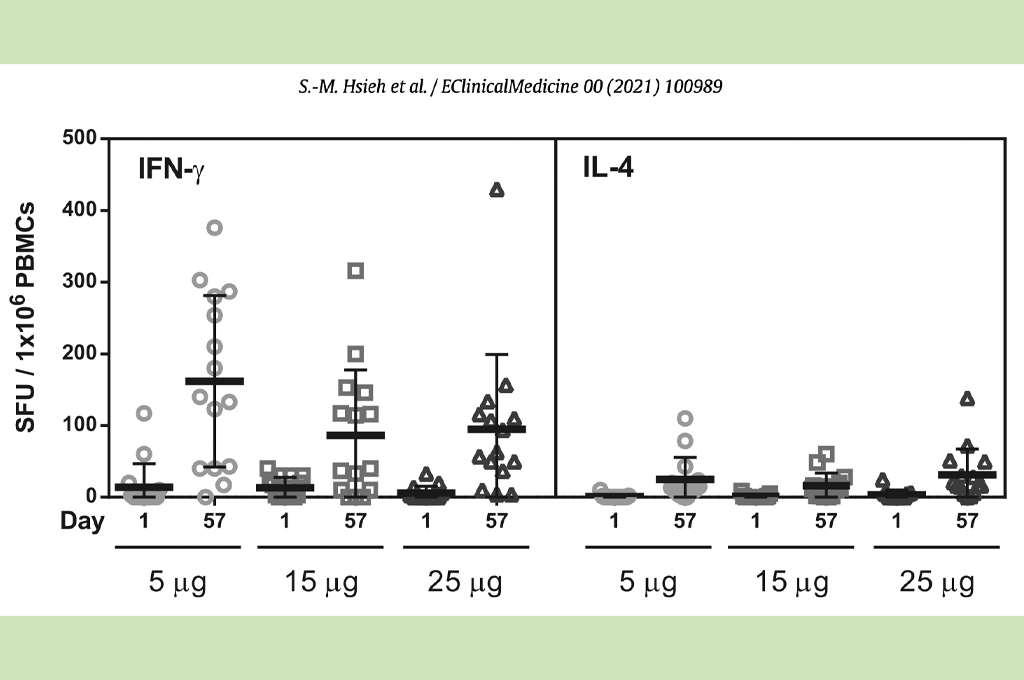
細胞免疫反應方面,研究顯示,所有參與者在基線時分泌干擾素伽瑪(IFN-g) 的T細胞最少。 直到第57天,在分別接種5毫克、15毫克、25毫克疫苗的參與者中,每100萬細胞中觀察到平均分泌161.3、85.5和94.9的T細胞。
研究補充,在接種疫苗之前,所有參與者的白细胞介(IL-4)分泌的T細胞最少。直到第57天,在分別接種5毫克、15毫克、25毫克疫苗的參與者中,每100萬細胞中觀察到平均分泌24.1、16.0和31.3的T細胞。
論文總結,高端疫苗具有良好的耐受性並能引發強大的免疫反應,適合進一步開發。
(圖片來源:《刺胳針》The Lancet、台大醫院官網)













